Resistencia antimicrobiana y fabricación farmacéutica: el papel del enfoque SSbD
La resistencia antimicrobiana (RAM) figura entre los principales retos de salud global del siglo XXI. Entre sus factores contribuyentes, los efluentes de la industria farmacéutica están recibiendo cada vez más atención. El enfoque Safe and Sustainable by Design (SSbD), junto con tecnologías de fabricación continua como la extrusión por fusión en caliente (HME) y la granulación en doble tornillo (TSG), permite minimizar estos residuos desde el origen del proceso productivo.
¿Qué es la resistencia antimicrobiana?
La resistencia antimicrobiana (RAM) es la capacidad de los microorganismos para sobrevivir o incluso proliferar en presencia de fármacos diseñados para inhibirlos o eliminarlos. Es una amenaza crítica para la salud global, con 10 millones de muertes causadas por la RAM y 1 billón de dólares estadounidenses en costes sanitarios adicionales proyectados para 2050. Además, las infecciones resistentes a los medicamentos afectan la salud de animales y plantas, reducen la productividad agrícola y amenazan la seguridad alimentaria.
La resistencia antimicrobiana se desarrolla principalmente en los microorganismos (como bacterias, virus, hongos y parásitos) a través de la exposición a fármacos antimicrobianos (incluidos antibióticos, antivirales, antifúngicos y antiparasitarios), lo que selecciona mutantes resistentes o facilita la adquisición de genes de resistencia.
¿Cuál es el impacto de la industria farmacéutica en la RAM?
Aunque la sobreprescripción y el uso inadecuado de antibióticos suelen estar en el centro del debate como factores principales, la exposición ambiental es cada vez más reconocida como un factor contribuyente.
El impacto directo de la fabricación farmacéutica en la prevalencia de la RAM aún no se ha cuantificado completamente, sin embargo, los efluentes de la industria farmacéutica contienen algunas de las concentraciones más altas de antibióticos y genes de resistencia a antibióticos detectados en el medio ambiente.
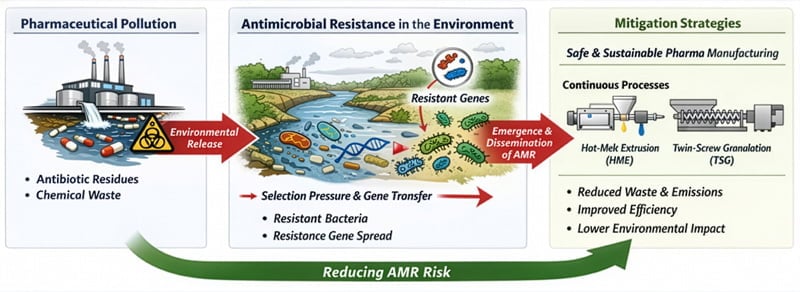
Una de las principales razones de esto es que la fabricación farmacéutica tradicional a menudo depende de procesos intensivos en disolventes (por ejemplo, granulación húmeda, cristalización), generando grandes volúmenes de aguas residuales y efluentes con disolventes. Cuando estos no se tratan adecuadamente, pueden contener principios activos farmacéuticos residuales en concentraciones suficientes para ejercer actividad biológica.
Incluso concentraciones subinhibitorias en los entornos receptores (aguas superficiales, sedimentos y suelos) pueden generar presión selectiva que favorece la proliferación de resistencias. La coexistencia de otros compuestos químicos puede agravar la RAM al crear presiones selectivas complejas que promueven la transferencia horizontal de genes y la supervivencia de microorganismos resistentes.
Además, actualmente no existen regulaciones plenamente armonizadas que establezcan límites específicos para antimicrobianos o concentraciones farmacéuticas más amplias en los efluentes industriales, como los procedentes de la fabricación farmacéutica. Los marcos regulatorios tradicionales se centran en niveles generales de contaminantes (por ejemplo, DBO, DQO) o en el control del uso de antimicrobianos, más que en regular directamente las descargas ambientales.
¿Qué es el enfoque SSbD y cómo reduce la contaminación por antibióticos?
La implementación de procesos de fabricación que minimicen los residuos es clave para reducir la contaminación ambiental y la presión selectiva que de ella se deriva. Este enfoque se basa en el marco “Safe and Sustainable by Design” (SSbD), un conjunto de principios que busca integrar estrategias de seguridad ambiental y sostenibilidad en todas las etapas del ciclo de vida de un medicamento, desde su diseño hasta su fabricación y su eliminación final.
En la fase de fabricación, las tecnologías emergentes que se alinean con el paradigma SSbD y pueden sustituir procesos por lotes intensivos en residuos son la extrusión por fusión en caliente y la granulación en extrusor de doble husillo.
HME y TSG: tecnologías de fabricación continua sin disolventes
- La Extrusión por Fusión en Caliente (Hot Melt Extrusion, HME) es un proceso de fabricación continuo en el que los fármacos y excipientes se funden y mezclan mediante calor y cizallamiento mecánico para formar una dispersión sólida homogénea, eliminando la necesidad de disolventes.
- La Granulación en Doble Tornillo (Twin-Screw Granulation, TSG) es un método continuo de granulación en el que los polvos se mezclan y aglomeran mecánicamente mediante tornillos gemelos, a menudo con un uso mínimo o nulo de aglutinantes líquidos, produciendo gránulos uniformes y reduciendo el uso de disolventes y el secado posterior. Las fortalezas de estas metodologías incluyen:
Ventajas de HME y TSG frente a los procesos tradicionales:
- Reducción de residuos: estas tecnologías pueden minimizar o sustituir completamente el uso de disolventes mediante mezclado térmico y mecánico.
- Mejor control del proceso: permiten la integración de monitorización en tiempo real mediante tecnología analítica de procesos (PAT), lo que reduce fallos de lote y productos fuera de especificación. Esto, a su vez, disminuye el volumen de materiales descartados.
- Menor consumo energético: las operaciones continuas suelen tener una menor intensidad energética por unidad producida, reduciendo emisiones y contribuyendo a una fabricación más sostenible y eficiente en costes.
Retos y perspectivas de futuro
La adopción de estos procesos de fabricación no está exenta de desafíos. Entre las barreras técnicas se incluyen la inversión en equipos, la ampliación de escala y la alineación regulatoria. Sin embargo, mediante la adopción de la fabricación continua alineada con los principios SSbD, las empresas farmacéuticas tienen una oportunidad única de abordar la RAM desde su origen, haciendo la producción más sostenible, eficiente y rentable.
¿Cómo apoya AIMPLAS la transición a la fabricación farmacéutica SSbD?
AIMPLAS puede apoyar la transición desde la fabricación por lotes tradicional hacia procesos continuos más sostenibles mediante investigación aplicada e infraestructura a escala piloto. Al tender puentes entre la investigación y la industria, facilitamos la adopción de tecnologías de fabricación continua mediante:
- Investigación a escala de laboratorio: utilizando procesos por lotes en estado sólido, evaluamos formulaciones que permiten una fabricación sin disolventes o con bajo uso de disolventes, reduciendo la posible generación de efluentes contaminados con antibióticos.
- Evaluación de la viabilidad técnica a escala pre-piloto: utilizando microextrusores (5–10 g/lote) y reómetros de torque (30–300 g/lote) optimizamos condiciones de procesamiento basadas en cizallamiento, apoyando la transición desde operaciones basadas en disolventes.
- Validación del proceso en condiciones industrialmente relevantes: utilizando extrusores de doble husillo en una sala limpia ISO 7 demostramos rutas de fabricación continua escalables.
¿Tu empresa está evaluando la transición hacia procesos de fabricación más sostenibles? Cuéntanos en qué punto del proceso estáis y analizamos juntos qué capacidades de AIMPLAS pueden encajar mejor. Contacta con AIMPLAS.
Referencias
World Health Organization. (retrieved march 2026). Antimicrobial resistance. https://www.who.int/news-room/fact-sheets/detail/antimicrobial-resistance
World Health Organization. (2022). Global antimicrobial resistance and use surveillance system (GLASS) report: 2022. https://www.who.int/publications/i/item/9789240062702